Загальна інформація
Сайт Моя Аптека є сучасною інформаційно-довідниковою платформою, яка допомагає знайти і порівняти ціни на будь-які товари аптечного асортименту в аптеках України. Це найпростіший спосіб підібрати ліки за найнижчою ціною в найближчій до Вас аптеці і заощадити до 20-30% на деяких покупках.
Переглядайте актуальні ціни та наявність необхідного товару в будь-якій аптеці на карті в онлайн форматі, бронюйте його всього в кілька кроків і забирайте в зручний час у зазначеній аптеці.
-
Як забронювати ліки на сайті Моя Аптека?
Оформити резерв на необхідний товар можна за допомогою зеленої кнопки із позначкою кошика «Забронювати» на сторінці товару, на карті або прямо з каталогу.
-
Чи можна отримати знижку при резервуванні?
Так! Наш сервіс дає можливість економити до 30% вартості від фактичної ціни в аптеці на ті товари, на які передбачена знижка. Сума знижки вказується при оформленні броні.
-
Як оплатити і отримати своє замовлення?
Оплата і отримання товару здійснюється тільки в аптеці за адресою, який був обраний при бронюванні товару. Моя Аптека дає можливість кожному економити гроші і час на покупці ліків.
Сайт mypharmacy.com.ua не надає послуг по доставці/відправленні товарів
Економте до 30% при бронюванні товарів в аптеках.
Депо-Провера суспензія д/ін., 150 мг/мл по 3,3 мл (500 мг) у флак. №1
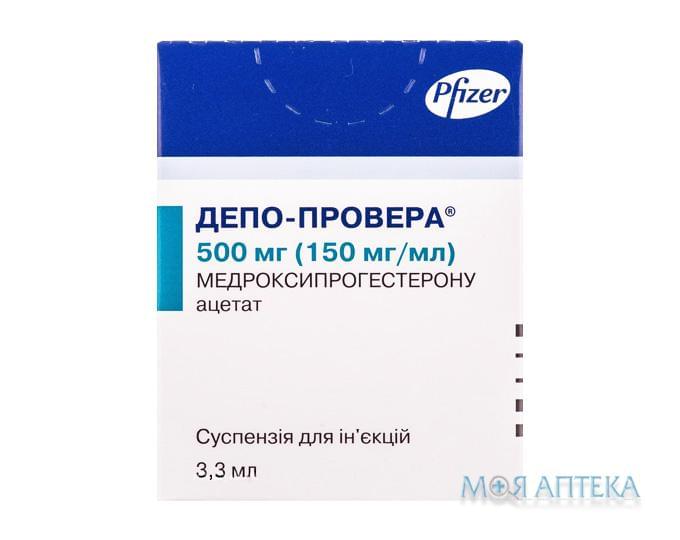
Наявність у 432 аптеках
Аптеки на мапіОсновна інформація
гормональна контрацепція
гінекологія
Ін’єкції
рецептурний
Інструкція для Депо-Провера суспензія д/ін., 150 мг/мл по 3,3 мл (500 мг) у флак. №1
- Склад
- Показання
- Протипоказання
- Спосіб застосування та дози
- Побічні реакції
- Передозування
- Застосування у період вагітності або годування груддю
- Умови зберігання
- Реєстраційні данні
Склад
діюча речовина: medroxyprogesterone;
1 мл суспензії містить медроксипрогестерону ацетату 150 мг;
допоміжні речовини: полісорбат 80, метилпарагідроксибензоат (E 218), пропілпарагідрокси-бензоат (E 216), макрогол 3350, натрію хлорид, вода для ін’єкцій.
Лікарська форма
Суспензія для ін’єкцій.
Основні фізико-хімічні властивості: суспензія білого кольору.
Фармакотерапевтична група
Гормональні контрацептиви для системного застосування. Гестагени. Код АТХ G03A C06.
Фармакологічні властивості
Фармакодинаміка.
Медроксипрогестерону ацетат чинить антиестрогенну, антиандрогенну та антигонадропічну дію.
Зміни мінеральної щільності кісткової тканини в дорослих жінок
Дослідження, у ході якого порівнювали зміни мінеральної щільності кісткової тканини в жінок, які застосовували препарат Депо-Провера®, та жінок, які отримували ін?єкції медроксипрогестерону ацетату (150 мг внутрішньом’язово), не продемонструвало значної відмінності у втраті мінеральної щільності кісткової тканини між двома групами після двох років лікування. Середні відсоткові значення змін мінеральної щільності кісткової тканини в групі прийому препарату Депо-Провера® наведені в таблиці 1.
Таблиця 1. Середнє відсоткове значення зміни мінеральної щільності кісткової тканини в жінок, які застосовували Депо-Провера®, за органами скелетної системи порівняно з початковим рівнем
|
Період лікування |
Поперековий відділ хребта |
Тазостегновий суглоб |
Шийка стегнової кістки |
|||
|
N |
Середній % зміни (95 % CІ) |
N |
Середній % зміни (95 % СІ) |
N |
Середній % зміни (95 % СІ) |
|
|
1-й рік |
166 |
(від -3,1 до -2,3) |
166 |
(від -2,1 до -1,3) |
166 |
(від -2,5 до -1,4) |
|
2-й рік |
106 |
(від -4,6 до -3,5) |
106 |
(від -4,2 до -2,7) |
106 |
(від -4,3 до -2,6) |
У ході іншого контрольованого клінічного дослідження з участю дорослих жінок, які застосовували ін?єкції медроксипрогестерону ацетату (150 мг внутрішньом’язово) протягом періоду до 5 років, було продемонстровано середнє зниження мінеральної щільності кісткової тканини хребта та стегна на 5-6 % порівняно з відсутністю значних змін у мінеральній щільності кісткової тканини у контрольній групі. Зниження мінеральної щільності кісткової тканини було більш виражене протягом перших 2-х років застосування та зменшувалося протягом наступних років. У середньому зміни мінеральної щільності кісткової тканини поперекового відділу хребта становили: -2,86 %, -4,11 %, -4,89 %, -4,93 % і -5,38 % після 1, 2, 3, 4 і 5 років відповідно. Середні значення зменшення мінеральної щільності кісткової тканини усієї стегнової кістки та її шийки були подібними. Додаткова інформація наведена у таблиці 2.
Після припинення застосування ін?єкцій медроксипрогестерону ацетату (150 мг внутрішньом’язово) мінеральна щільність кісткової тканини збільшувалася порівняно з початковими значеннями протягом післятерапевтичного періоду. Більш тривале лікування пов?язувалося зі зниженням швидкості відновлення мінеральної щільності кісткової тканини.
Таблиця 2. Середнє відсоткове значення зміни мінеральної щільності кісткової тканини порівняно з початковим рівнем у дорослих жінок за органами скелетної системи після 5 років проведення терапії медроксипрогестерону ацетатом 150 мг внутрішньом’язово та через 2 роки після припинення застосування або 7 років спостереження (контрольна група)
|
Період проведен-ня досліджен-ня |
Хребет |
Стегнова кістка у цілому |
Шийка стегнової кістки |
|||
|
Медрокси-прогестеро-ну ацетат |
Контроль |
Медрокси-прогестеро-ну ацетат |
Контроль |
Медрокси-прогестеро-ну ацетат |
Контроль |
|
|
5 років* |
n = 33
|
n = 105 0,43 % |
n = 21
|
n = 65 0,19 % |
n = 34
|
n = 106
|
|
7 років** |
n = 12
|
n = 60 0,53 % |
n = 7
|
n = 39 0,94 % |
n = 13
|
n = 63
|
* – група лікування складалася з жінок, які застосовували ін?єкції медроксипрогестерону ацетату (150 мг внутрішньом’язово) протягом 5 років, та контрольної групи, що складалася з жінок, які не застосовували засоби гормональної контрацепції протягом цього періоду.
** – група лікування складалася з жінок, які застосовували ін?єкції медроксипрогестерону ацетату (150 мг внутрішньом’язово) протягом 5 років і проходили подальше спостереження протягом 2 років після закінчення терапії, та контрольної групи, що складалася з жінок, які не застосовували засоби гормональної контрацепції протягом 7 років.
Зміни мінеральної щільності кісткової тканини у дівчат-підлітків (12-18 років)
Результати відкритого нерандомізованого клінічного дослідження ін?єкцій медроксипрогестерону ацетату (150 мг внутрішньом’язово кожні 12 тижнів протягом 240 тижнів (4,6 року) та подальшим післятерапевтичним контролем показників) у дівчат-підлітків (12-18 років) також продемонстрували, що застосування медроксипрогестерону ацетату внутрішньом’язово пов?язане зі значним зниженням мінеральної щільності кісткової тканини відносно початкового рівня. Серед пацієнток, яким застосовували ≥4 ін?єкцій на 60-тижневий період, середнє зниження мінеральної щільності кісткової тканини поперекового відділу хребта становило -2,1 % після 240 тижнів (4,6 року); середнє зниження для стегнової кістки та шийки стегна становило -6,4 % і -5,4 % відповідно. Післятерапевтичний нагляд продемонстрував (на основі середніх значень), що мінеральна щільність кісткової тканини поперекового відділу хребта відновилася до початкового рівня приблизно через 1 рік після припинення лікування, а мінеральна щільність кісткової тканини стегнової кістки відновилася до початкового рівня приблизно через 3 роки після припинення лікування. Проте важливо зазначити, що велика кількість пацієнток припинила свою участь у дослідженні. Таким чином, результати базуються на невеликій кількості пацієнток (n = 71 через 60 тижнів і n = 25 через 240 тижнів після припинення лікування). З іншого боку, неспівставна група розрізнених пацієнток, які не проходили терапію, з різними показниками кісткової маси на початковому рівні порівняно з пацієнтками, які застосовували медроксипрогестерону ацетат, продемонструвала в середньому збільшення мінеральної щільності кісткової тканини через 240 тижнів для поперекового відділу хребта, стегнової кістки та шийки стегна, що становило 6,4 %, 1,7 % і 1,9 % відповідно.
Фармакокінетика.
Парентеральний медроксипрогестерону ацетат – це прогестаційний стероїд довготривалої дії. Довготривала дія відбувається за рахунок повільної абсорбції препарату з місця ін?єкції. Одразу після ін?єкції 150 мг/мл медроксипрогестерону ацетату його рівні у плазмі крові становили 1,7 ± 0,3 нмоль/л. Через 2 тижні рівні становили 6,8 ± 0,8 нмоль/л. Концентрації поверталися до початкових рівнів під кінець 12 тижнів. У разі низьких доз рівні медроксипрогестерону ацетату у плазмі крові вважаються такими, що безпосередньо залежать від застосованої дози. Накопичення в сироватці крові з часом не було продемонстроване. Медроксипрогестерону ацетат виводиться з калом або сечею. Період напіввиведення з плазми крові становить приблизно 6 тижнів після однієї внутрішньом?язової ін?єкції. Повідомлялося про щонайменше 11 метаболітів. Усі виводяться з сечею, деякі (проте не всі) – у кон?югованій формі.
Показання
Прогестоген: для контрацепції.
Депо-Провера® є засобом довготривалої контрацепції, придатним для застосування жінкам, яких було відповідним чином проінформовано щодо можливості виникнення менструальних розладів і потенційної затримки відновлення повної фертильності.
Препарат Депо-Провера® можна також застосовувати для короткотривалої контрацепції в таких випадках:
1) для партнерок чоловіків, які перенесли вазектомію, для захисту, доки вазектомія не стане ефективною;
2) жінкам, імунізованим проти краснухи, для запобігання вагітності під час періоду активності вірусу;
3) жінкам, які очікують на стерилізацію.
Діти (12-18 років)
Препарат Депо-Провера® не призначають для застосування до настання менструального періоду.
Препарат можна застосовувати підліткам, але тільки якщо інші методи контрацепції визнані непридатними або неприйнятними після їх обговорення з пацієнткою.
Доступні дані щодо застосування препарату дівчатами-підлітками (12-18 років) (див. розділ «Особливості застосування»). Якщо це не стосується втрати мінеральної щільності кісткової тканини, безпека та ефективність препарату Депо-Провера® в дівчат-підлітків після настання менструального періоду очікуються такими ж, як і в дорослих жінок.
Протипоказання
Препарат Депо-Провера® протипоказаний пацієнткам із відомою чутливістю до медроксипрогестерону ацетату або до будь-яких інших компонентів препарату.
Застосування препарату як контрацептива у наведеному нижче дозуванні протипоказане при наявності підтверджених або підозрюваних гормонозалежних злоякісних пухлин молочної залози або статевих органів.
Препарат Депо-Провера® протипоказаний пацієнткам з наявністю або анамнезом тяжких захворювань печінки, у яких показники функції печінки не повернулися до норми.
При призначенні як монотерапії чи в комбінації з естрогенами препарат Депо-Провера® не слід застосовувати пацієнткам з патологічною матковою кровотечею, поки не буде з’ясований діагноз і не буде виключена можливість наявності злоякісних пухлин статевих шляхів.
Взаємодія з іншими лікарськими засобами та інші види взаємодій
Застосування аміноглутетиміду одночасно з препаратом Депо-Провера® може значно пригнічувати біодоступність останнього.
Про випадки взаємодії з іншими лікарськими засобами повідомлялося рідко (включаючи пероральні антикоагулянти), але причини такої взаємодії не були визначені. Слід прийняти до уваги можливість взаємодії у пацієнток, для лікування яких одночасно застосовують інші лікарські засоби.
Кліренс медроксипрогестерону ацетату приблизно дорівнює швидкості печінкового кровообігу. Завдяки цьому факту малоймовірно, що препарати, які індукують ензими печінки, будуть значно впливати на кінетику медроксипрогестерону ацетату. Тому не рекомендується корекція дози у пацієнток, які приймають препарати, відомі своїм впливом на печінкові метаболізуючі ферменти.
Медроксипрогестерону ацетат первинно метаболізується in vitro реакцією гідроксилювання за допомогою CYP3A4. Спеціальних досліджень із взаємодії між лікарськими засобами, що б оцінили клінічний ефект індукторів або інгібіторів CYP3A4 на медроксипрогестерону ацетат, не проводилося, а отже, клінічний ефект індукторів або інгібіторів CYP3A4 невідомий.
Особливості застосування
Втрата мінеральної щільності кісткової тканини
Застосування препарату Депо-Провера® знижує рівні естрогену в сироватці крові та пов?язується зі значною втратою мінеральної щільності кісткової тканини через відомий ефект недостатності естрогену на систему відновлення кісткової тканини. Втрата кісткової маси збільшується при тривалому застосуванні препарату, проте виявляється, що після припинення застосування препарату мінеральна щільність кісткової тканини збільшується, а також підвищується продукування естрогену в яєчниках.
Втрата мінеральної щільності кісткової тканини являє собою особливу проблему для підлітків та дорослих молодшого віку під час критичного періоду приросту кісткової маси. Невідомо, чи зменшить застосування препарату Депо-Провера® пікову кісткову масу в жінок молодшого віку та чи підвищить ризик переломів у подальшому житті.
Дослідження з оцінки впливу застосування медроксипрогестерону ацетату (Депо-Провера®) внутрішньом’язово на мінеральну щільність кісткової тканини в дівчат-підлітків продемонструвало, що застосування пов?язується зі значним зменшенням мінеральної щільності кісткової тканини порівняно з початковим рівнем. У невеликої кількості жінок, які проходили подальше спостереження, значення мінеральної щільності кісткової тканини в середньому відновилися до значень на початковому рівні через 1-3 роки після припинення застосування. Препарат Депо-Провера® можна застосовувати для підлітків, але тільки якщо інші методи контрацепції визнані непридатними або неприйнятними після їх обговорення з пацієнтками.
Для жінок усіх вікових категорій слід ретельно зважити ризики та користь від лікування, якщо їм потрібно застосовувати препарат більше двох років. Зокрема, при наявності значних факторів ризику способу життя та/або медичних факторів ризику, що можуть спричинити остеопороз, для жінок слід розглянути інші засоби контрацепції перед застосуванням препарату Депо-Провера®.
Значні фактори ризику виникнення остеопорозу включають:
- зловживання алкоголем або паління;
- постійне застосування препаратів, що можуть зменшити кісткову масу, наприклад протисудомних препаратів або кортикостероїдів;
- низький індекс маси тіла або порушення харчування, наприклад нервово-психічна анорексія або булімія;
- попередній перелом у результаті падіння з висоти свого росту;
- остеопороз у сімейному анамнезі.
За результатами ретроспективного дослідження груп на основі даних з бази досліджень загальної лікарської практики (GPRD) ризик переломів у жінок, яким застосовували ін?єкції медроксипрогестерону ацетату, вищий, ніж у жінок, які застосовували контрацептиви з незареєстрованим застосуванням медроксипрогестерону ацетату (співвідношення частоти виникнення становило 1,41, 95 % СІ 1,35-1,47 протягом періоду подальшого спостереження тривалістю 5 років. Невідомо, чим саме ця частота переломів була спричинена: медроксипрогестерону ацетатом чи іншими відповідними факторами способу життя. З іншого боку, у жінок, які застосовують медроксипрогестерону ацетат, ризик виникнення переломів до та після початку застосування цього препарату не підвищився (відносний ризик 1,08; 95 % СІ 0,92-1,26). Важливо зазначити, що це дослідження не змогло визначити наявність впливу на частоту виникнення переломів у подальшому житті.
Додаткову інформацію про зміни мінеральної щільності кісткової тканини як у дорослих, так і в дівчат-підлітків (за звітами нещодавніх клінічних досліджень) див. у розділі «Фармакодинаміка». Для здоров?я кісток жінкам будь-якого віку важливо застосовувати належний об?єм кальцію та вітаміну D (або з добавками, або з відповідною дієтою).
Нерегулярні менструації
Зазвичай застосування препарату Депо-Провера® спричиняє порушення нормального менструального циклу. Особливості кровотечі включають аменорею (зазнають до 30 % жінок протягом перших 3 місяців, частка збільшується до 55 % та 68 % на 12-му та 24-му місяці відповідно); нерегулярні кровотечі та кровомазання; епізоди довготривалої (більше 10 днів) кровотечі (зазнають до 33 % жінок протягом перших 3 місяців застосування, частка зменшується до 12 % на 12-му місяці). У поодиноких випадках можуть відбуватися тяжкі довготривалі кровотечі. Свідчення дозволяють припустити, що довготривалі або тяжкі кровотечі, що потребують лікування, можуть виникнути в 0,5-4 випадках на 100 пацієнто-років застосування. Якщо аномальні кровотечі продовжуються або набувають тяжкої форми, слід провести відповідне обстеження на можливість патології органів і при необхідності розпочати відповідне лікування. Надмірну або довготривалу кровотечу можна контролювати одночасним застосуванням низької дози естрогену (30 мікрограм) разом з пероральними контрацептивами або у формі замісної терапії естрогеном, наприклад кон?югованим кінським естрогеном (0,625-1,25 мг на добу). У разі необхідності терапію естрогеном слід повторити ще протягом 1-2 циклів. Довготривале супутнє застосування естрогену не рекомендується.
Відновлення репродуктивної функції
Немає свідчень про те, що Депо-Провера® безповоротно спричиняє безплідність. Вагітність виникала на 14-му тижні після попередньої ін?єкції, проте у клінічних дослідженнях середній час відновлення овуляції становив 5,3 місяця після попередньої ін?єкції. Жінкам слід повідомити, що існує імовірність затримки повного відновлення репродуктивної функції після застосування цього засобу незалежно від тривалості застосування, проте 83 % жінок можуть очікувати зачаття протягом 12 місяців після першої «пропущеної» ін?єкції (тобто через 15 місяців після останньої проведеної ін?єкції). Середній термін настання зачаття становив 10 місяців (у діапазоні від 4 до 31) після останньої ін?єкції.
Ризик виникнення раку
Довготривалі спостереження у випадках контрольованого застосування препарату Депо-Провера®виявили слабкий або не показали загального збільшення ризику виникнення раку молочної залози і не показали загального збільшення ризику виникнення раку яєчників, печінки або шийки матки; та виявили довготривалий захисний ефект, що полягає у зменшенні ризику виникнення раку ендометрія у популяції пацієнток, які застосовували препарат.
Рак молочної залози рідко виникає у жінок віком до 40 років, незалежно від того, користуються вони гормональними контрацептивами чи ні.
Результати деяких епідеміологічних досліджень дають змогу припустити наявність невеликої різниці у ризику виникнення захворюваності між пацієнтками, які ніколи не застосовували цей засіб контрацепції, і тими, які застосовують або нещодавно застосовували його. Будь-яке збільшення ризику для пацієнток, які застосовують або нещодавно застосовували медроксипрогестерону ацетат, невелике порівняно із загальним ризиком виникнення раку молочної залози, особливо серед молодих жінок (див. нижче), і підвищений ризик поступово зникає після 10 років від застосування останньої дози препарату. Тривалість застосування не вважається важливою.
Можлива кількість додаткових випадків виникнення раку молочної залози, діагностованих протягом періоду до 10 років після припинення застосування ін?єкцій прогестогенів*
|
Вік застосування останньої дози препарату Депо-Провера® |
Кількість випадків на 10 000 жінок, які ніколи не застосовували контрацептив |
Можлива кількість додаткових випадків на 10 000 жінок, які застосовували препарат Депо-Провера® |
|
20 |
Менше 1 |
Набагато менше 1 |
|
30 |
44 |
2-3 |
|
40 |
160 |
10 |
* – на основі застосування протягом 5 років
Відмічалося збільшення ризику виникнення раку молочної залози при застосуванні комбінованих оральних контрацептивів (естроген/прогестин) жінками у період постменопаузи. Результати рандомізованих плацебо-контрольованих досліджень та епідеміологічних досліджень повідомляли про збільшення ризику виникнення раку молочної залози у жінок, які приймали комбіновані естроген/прогестин препарати для гормональної терапії протягом кількох років. Було відмічено, що застосування естрогену в комбінації з прогестином призводило до збільшення аномальних мамограм, що потребувало подальшого обстеження.
У кількох епідеміологічних дослідженнях не було виявлено загального збільшення ризику виникнення раку молочної залози серед осіб, які застосовували депо-ін’єкції прогестогенів, у порівнянні з тими, які їх не застосовували. Однак, було відмічено підвищений відносний ризик (наприклад 2.0 в одному дослідженні) для жінок, які застосовували депо-ін’єкції прогестогенів на той час або застосовували їх лише за кілька років перед тим.
З цих даних неможливо зробити висновок, чи цей підвищений коефіцієнт діагностики раку молочної залози серед осіб, які застосовували препарат на той час, є результатом підвищеного контролю за тими пацієнтками, біологічного впливу ін’єкційних прогестогенів, чи поєднання цих причин.
У деяких епідеміологічних дослідження поточне застосування лише естрогену або естрогену у поєднанні з продуктами прогестину жінками у період постменопаузи протягом п’яти або більше років було пов’язане з підвищеним ризиком виникнення раку яєчників. Після припинення застосування лише естрогену або естрогену у поєднанні з продуктами прогестину у пацієнток не було ризику виникнення раку яєчників. Інші дослідження не показали значного зв’язку або ризик був статистично незначний. У одному дослідженні жінки, які отримували гормональну терапію, мали підвищений ризик летального раку яєчників.
Збільшення маси тіла
Існує тенденція до збільшення маси тіла в жінок під час терапії препаратом Депо-Провера®. Дослідження вказують на те, що протягом перших 1-2 років застосування середнє збільшення маси становило 5-8 фунтів (приблизно 2-4 кг). У жінок після терапії протягом 4-6 років середнє збільшення маси становило 14-16,5 фунта (приблизно 6-7,5 кг). Існують докази, що збільшення маси тіла відбувається в результаті збільшення маси жирової тканини і не є вторинним проявом анаболічного ефекту або затримки рідини.
Анафілаксія
Були отримані звіти про анафілактичні відповіді (анафілактичні реакції, анафілактичний шок, анафілактоїдні реакції).
Тромбоемболічні порушення
Якщо під час застосування препарату Депо-Провера®в пацієнток виникла легенева емболія, цереброваскулярна хвороба або тромбоз сітківки, препарат не слід застосовувати повторно.
Психічні порушення
Пацієнткам із випадками ендогенної депресії в анамнезі слід знаходитися під ретельним наглядом. Під час терапії препаратом Депо-Провера® деякі пацієнтки можуть скаржитися на депресію передменструального типу.
Утворення абсцесу
Як і для будь-якої внутрішньом’язової ін’єкції, особливо якщо вона була виконана неправильно, існує ризик утворення абсцесу у місці проведення ін’єкції, що може потребувати медичного та/або хірургічного втручання.
Застереження
Наявність в анамнезі або виникнення наступних станів потребує особливої уваги та відповідних обстежень: мігрень або незвичний сильний головний біль, гострі порушення зору будь-якого виду, патологічні зміни функції печінки або гормонального балансу.
Пацієнток з тромбоемболічним захворюванням або захворюванням коронарних судин слід ретельно обстежити перед застосуванням препарату Депо-Провера®.
Зниження толерантності до глюкози може спостерігатися у деяких пацієнток під час лікування прогестогенами. Механізм цього зниження незрозумілий. З цієї причини за пацієнтами, хворими на цукровий діабет, слід ретельно спостерігати під час отримання терапії прогестогенами.
Повідомлялося про поодинокі випадки тромбоемболії при застосуванні препарату Депо-Провера®, але причинний зв'язок не був встановлений.
Якщо при обстеженні виявлено набряк диску зорового нерва або ураження сітківки, лікування не повинно призначатися повторно.
Вивчення впливу медроксипрогестерону ацетату на метаболізм ліпідів не виявило чіткої взаємодії. Під час досліджень спостерігалося як збільшення, так і зменшення рівня загального холестерину, тригліцеридів та холестерину ліпопротеїнів низької щільності (ЛПНЩ).
Застосування Депо-Провера® пов’язано зі зменшенням на 15-20 % рівня холестерину ліпопротеїнів високої щільності у сироватці крові (ЛПВЩ), що може захистити жінку від кардіоваскулярних порушень. Клінічні наслідки цього спостереження невідомі. До застосування препарату необхідно розглянути можливість підвищеного ризику виникнення ішемічної хвороби серця.
Лікарям необхідно ретельно обміркувати застосування Депо-Провера® хворим, у яких нещодавно виникла трофобластична хвороба, поки рівні хоріонічного гонадотропіну людини не повернулися до норми.
Лікарі повинні бути проінформовані про те, що необхідно попередити патогістолога про застосування пацієнткою Депо-Провера®, якщо ендометріальна або ендоцервікальна тканина надається для дослідження.
Застосування Депо-Провера®може впливати на результати деяких лабораторних тестів, включаючи рівень гонадотропінів (знижений), рівень прогестерону у плазмі крові (знижений), рівень прегнандіолу в сечі (знижений), рівень естрогенів у плазмі крові (знижений), рівень кортизолу в плазмі крові (знижений), тест толерантності до глюкози, тест з метирапоном, функціональні печінкові тести (можуть бути підвищені), тести на функцію щитовидної залози (рівень зв’язування йоду протеїнами може бути підвищеним та рівень поглинання ТЗ може зменшуватися). Показники коагулограми для протромбіну (Фактор ІІ) і Фактори VII, VIII, IX і X можуть зростати.
У зв’язку з тим, що втрата мінеральної щільності кісток може виникнути у жінок будь-якого віку, які тривалий час застосовують ін’єкції препарату Депо-Провера® (див. розділ «Особливості застосування»), при призначенні препарату необхідно розглянути співвідношення ризик/користь з урахуванням зменшення мінеральної щільності кісток, що відбувається протягом періоду вагітності та/або годування груддю.
Дуже важливо надати потенційним пацієнткам адекватні пояснення стосовно довготривалої дії препарату, можливих побічних ефектів і неможливості негайного усунення наслідків дії кожної ін’єкції, а також докласти усіх зусиль для того, щоб переконатися, що кожна пацієнтка одержала необхідні рекомендації, які дають їй можливість повністю зрозуміти ці пояснення.
Відповідно до належної клінічної практики перед призначенням препарату Депо-Провера® та через відповідні проміжки часу слід провести загальний медичний огляд, а також гінекологічне обстеження.
Спосіб застосування та дози
Щоб упевнитися, що доза, яка застосовується, являє собою однорідну суспензію препарату Депо-Провера®, суспензію для ін’єкцій слід ретельно збовтати безпосередньо перед застосуванням.
Дози потрібно вводити шляхом глибокої внутрішньом’язової ін’єкції. Слід бути впевненими у тому, що депо-ін’єкція проведена у м’язову тканину, бажано у великий сідничний м’яз, але також можна використати інші м’язи, наприклад дельтоподібний.
Перед проведенням ін’єкції слід очистити місце ін’єкції, використовуючи для цього стандартні методи.
Дорослі
Перша ін?єкція: для забезпечення контрацептивного ефекту протягом першого циклу застосування слід провести ін’єкцію 150 мг препарату внутрішньом’язово протягом перших 5 діб нормального менструального циклу. Якщо ін’єкція була проведена згідно з цією інструкцією, застосування додаткових контрацептивних засобів не потрібне.
Після пологів: для збільшення впевненості, що пацієнтка не є вагітною на час першого застосування препарату, ін’єкцію слід здійснити протягом 5 днів після пологів, якщо жінка не годує груддю.
Існують дані, які вказують на те, що у жінок, які застосовують Депо-Провера® безпосередньо у післяпологовий період, може виникнути тривала і тяжка кровотеча. З цієї причини у післяпологовий період препарат слід застосовувати з обережністю. Жінок, які вирішили застосовувати препарат безпосередньо після пологів або після переривання вагітності, слід проінформувати про підвищений ризик виникнення тяжкої або тривалої кровотечі. Лікарям потрібно нагадати, що у жінок, які не годують груддю, овуляція може відбуватися вже на 4 тиждень після пологів.
Якщо жінка після пологів буде годувати дитину груддю, першу ін’єкцію слід проводити не раніше, ніж через 6 тижнів після пологів, коли ферментативна система новонародженого повніше розвинута. Подальші ін’єкції слід проводити з інтервалами у 12 тижнів.
Подальші дози: слід застосовувати з інтервалом у 12 тижнів, однак якщо ін’єкцію вводити не пізніше ніж через 5 днів після цього часу, додаткові заходи контрацепції не потрібні (наприклад, бар’єрні). (Примітка: для партнерок чоловіків, які перенесли вазектомію, може бути необхідна друга ін’єкція 150 мг препарату внутрішньом’язово через 12 тижнів після першої. Це може бути необхідним для невеликої кількості пацієнток, у партнерів яких кількість сперматозоїдів не впала до нуля). Якщо з будь-якої причини час від проведення попередньої ін’єкції перевищує 89 днів (12 тижнів і 5 днів), перед наступною ін’єкцією слід виключити вагітність, а пацієнтці слід застосовувати додаткові заходи контрацепції (наприклад, бар’єрні) протягом 14 днів після проведення цієї наступної ін’єкції.
Пацієнти літнього віку: не застосовується.
Перехід з інших засобів контрацепції
Препарат Депо-Провера® слід застосовувати так, щоб забезпечити безперервну контрацептивну дію. Для цього слід зважати на механізм дії інших засобів (наприклад, пацієнткам, які переходять з пероральних контрацептивів, слід ввести першу ін?єкцію препарату протягом 7 днів після застосування останньої активної таблетки).
Печінкова недостатність
Ефект захворювання печінки на фармакокінетику препарату Депо-Провера® невідомий. Оскільки препарат здебільшого виводиться через печінку, його метаболізм може бути слабким у пацієнток з тяжкою печінковою недостатністю (див. розділ «Протипоказання»).
Ниркова недостатність
Ефект захворювання нирок на фармакокінетику препарату Депо-Провера® невідомий. У жінок з нирковою недостатністю коригування дози не потрібне, оскільки препарат Депо-Провера® майже повністю виводиться через метаболізм у печінці.
Діти.
Препарат Депо-Провера® не призначати для застосування до настання менструального періоду (див. розділ «Показання»).
Доступні дані щодо застосування препарату дівчатами-підлітками (12-18 років) (див. розділ «Особливості застосування»). Якщо це не стосується втрати мінеральної щільності кісткової тканини, безпека та ефективність препарату Депо-Провера® в дівчат-підлітків після настання менструального періоду очікуються такими ж, як і в дорослих жінок.
Побічні реакції
Під час проведення великого клінічного дослідження з участю понад 3900 жінок, які застосовували Депо-Провера® протягом 7 років, повідомлялося про наведені нижче побічні ефекти.
Наступні побічні реакції було відзначено як часті (більше ніж у 5 % пацієнток): нерегулярні менструації (кровотеча та/або аменорея), зміна маси тіла, головний біль, нервозність, біль або дискомфорт у животі, запаморочення, астенія (слабкість або швидка втомлюваність).
Побічні реакції, що були відзначені в 1-5 % пацієнток, які застосовували Депо-Провера®, були такими: зниження лібідо або аноргазмія, біль у спині, судоми ніг, депресія, нудота, безсоння, лейкорея, акне, вагініт, біль у ділянці таза, біль у грудях, відсутність росту волосся або алопеція, здуття живота, висипання, набряк, гарячі припливи.
Побічні реакції зазначені за вказаними нижче категоріями.
Дуже часто: >10 %.
Часто: від ≥1 % до <10 %.
Нечасто: від >0,1 % до <1 %.
Рідко: <0,1 %.
Невідомо (частота не може бути встановлена на підставі наявних даних).
З боку органів слуху та вестибулярного апарату
Нечасто: вертиго.
З боку шлунково-кишкового тракту
Дуже часто: біль або дискомфорт у животі.
Часто: здуття живота, нудота.
Нечасто: метеоризм, шлунково-кишкові розлади.
Рідко: ректальна кровотеча.
Інфекції та інвазії
Часто: вагініт.
Метаболічні та аліментарні розлади
Часто: зниження апетиту, підвищення апетиту.
Нечасто: збільшення маси тіла, зменшення маси тіла, затримка рідини.
З боку опорно-рухового апарату та сполучної тканини
Часто: біль у спині.
Нечасто: артралгія, м?язові спазми, біль у кінцівках.
Невідомо: остеопороз, включаючи остеопоротичні переломи, зниження щільності кісткової тканини, пахвові набряки.
З боку нервової системи
Дуже часто: головний біль.
Часто: запаморочення.
Нечасто: сонливість, мігрень, судоми.
Рідко: параліч.
Невідомо: синкопе.
З боку репродуктивної системи та молочних залоз
Часто: аменорея, біль/болісність у грудях, міжменструальні кровотечі, менометрорагія, менорагія, біль у ділянці таза, лейкорея.
Нечасто: вагінальні виділення, вульвовагінальна сухість, дисменорея, зміни розміру молочних залоз, диспаренурія, кіста яєчників, передменструальний синдром, інфекції сечостатевих шляхів, гіперплазія матки.
Рідко: ущільнення молочних залоз або кровотеча із соска.
Невідомо: патологічна маткова кровотеча (нерегулярна, підвищена, знижена), галакторея, вагінальна кіста, перешкодження лактації, відчуття симптомів як при вагітності, відсутність відновлення репродуктивної функції.
Існує можливість розвитку ерозії шийки матки, тривалої ановуляції.
З боку судин
Часто: гарячі припливи.
Нечасто: артеріальна гіпертензія, варикозне розширення вен, тромбофлебіт, легенева емболія.
Невідомо: тромбоемболічні розлади, тромбоз глибоких вен.
З боку серцево-судинної системи
Рідко: тахікардія.
З боку імунної системи
Нечасто: реакції гіперчутливості (наприклад анафілаксія та анафілактоїдні реакції, ангіоневротичний набряк).
З боку гепатобіліарної системи
Нечасто: патологічний рівень печінкових ферментів, жовтяниця.
Невідомо: порушення функції печінки.
Розлади з боку шкіри та підшкірної клітковини
Часто: акне, алопеція, висипання.
Нечасто: хлоазма, дерматит, екхімози, гірсутизм, свербіж, мелазма, кропив?янка, набряк.
Невідомо: розтяжки шкіри, склеродерма.
Загальні розлади та реакції у місці введення
Часто: підвищена втомлюваність, реакції у місці ін?єкції (включаючи біль або абсцес), астенія, парестезія.
Нечасто: біль у грудній клітці, гарячка.
Рідко: відчуття спраги, дисфонія, параліч.
Невідомо: параліч лицевого нерва.
Результати досліджень
Нечасто: аномальний мазок із шийки матки.
Рідко: зниження переносимості глюкози.
Психічні порушення
Часто: аноргазмія, депресія, нервозність, емоційний розлад, зниження лібідо, розлад настрою, дратівливість, безсоння.
Нечасто: тривожність.
Доброякісні, злоякісні та неспецифічні новоутворення (включаючи кісти та поліпи)
Рідко: рак молочної залози.
З боку системи крові та лімфатичної системи
Рідко: анемія.
Невідомо: дискразія крові.
З боку дихальної системи, грудної клітки та середостіння
Нечасто: задишка.
Звітування про підозрювані побічні реакції
Звітування про підозрювані побічні реакції після реєстрації лікарського засобу має важливе значення. Це дає змогу проводити безперервний моніторинг співвідношення між користю і ризиками, пов?язаними із застосуванням цього лікарського засобу. Медичних працівників просять звітувати про будь-які підозрювані побічні реакції.
Передозування
Не вимагаються ніякі спеціальні заходи, окрім припинення терапії.
Застосування у період вагітності або годування груддю
Препарат Депо-Провера® не слід застосовувати у період вагітності ні для діагностики, ні для лікування. Препарат протипоказаний вагітним жінкам.
Лікарям необхідно перевірити пацієнток на наявність вагітності перед проведенням першої ін’єкції Депо-Провера®, а також чи не було затримане будь-яке наступне застосування ін?єкції понад 89 днів (12 тижнів та 5 днів).
Діти, народжені внаслідок випадкової вагітності, що наставала через 1-2 місяці після ін’єкції Депо-Провера® , мали вищий ризик народження з низькою масою тіла, що у свою чергу пов’язано з більш високим ризиком неонатальної летальності. Відповідний ризик низький, тому що такі вагітності є рідкісними.
У дітей, які зазнали впливу медроксипрогестерону ацетату in utero та за якими проводили спостереження до підліткового віку, не було відзначено жодного побічного впливу на здоров?я, у тому числі на фізичний, інтелектуальний, статевий або соціальний розвиток.
Медроксипрогестерону ацетат та/або його метаболіти проникають у грудне молоко, але немає даних, що дозволяють вважати, що це становить небезпеку для дитини. Проводилося дослідження немовлят, які зазнали впливу медроксипрогестерону ацетату в період годування грудним молоком, щодо впливу на розвиток і поведінку до пубертатного періоду. Побічні реакції не відзначені.
Здатність впливати на швидкість реакції при керуванні автотранспортом або іншими механізмами.
Застосування препарату Депо-Провера® може спричинити певні побічні ефекти, здатні впливати на нервову систему. При наявності таких ефектів пацієнткам рекомендується уникати керування автотранспортом або роботи з іншими механізмами.
Умови зберігання
Зберігати при температурі не вище 25 °С у недоступному для дітей місці. Не заморожувати.
Термін придатності
5 років.
Упаковка
По 1 мл суспензії у флаконі або заповненому шприці, по 1 флакону або 1 шприцу в картонній коробці.
Категорія відпуску
за рецептом.
Реєстраційні данні
Інструкція для: Депо-Провера суспензія д/ін., 150 мг/мл по 3,3 мл (500 мг) у флак. №1
Виробник: Пфайзер Менюфекчуринг Бельгія Н.В., Бельгія/США
Фарм. група: Гормональні контрацептиви для системного застосування. Гестагени.
Реєстрація: № UA/0499/01/01 від 30.01.2014. Наказ № 88 від 30.01.2014
МНН: Medroxyprogesterone
Код АТХ:
(G) Лікарські засоби для лікування захворювань урогенітальних органів та статеві гормони
(G03) Статеві гормони та модулятори статевої системи
(G03A) Гормональні контрацептиви для системного застосування
(G03AC) Прогестогени (гестогени)
(G03AC06) Медроксипрогестерон
Всі варіанти товару:






Відгук про Депо-Провера суспензія д/ін., 150 мг/мл по 3,3 мл (500 мг) у флак. №1
Цей товар ще не має відгуків